I trombi sanguigni rari possono essere considerati un effetto collaterale “molto raro” del vaccino di AstraZeneca contro il Covid-19, ma i benefici del siero continuano a essere superiori ai rischi. È questa la conclusione dell’Ema dopo l’analisi su 86 casi rilevati su circa 25 milioni di europei vaccinati con il rimedio anglo-svedese. Nello stesso giorno in cui l’Oms ha appurato che un nesso causale fra il vaccino di AstraZeneca e i casi rari di trombi sanguigni associati a livelli bassi di piastrine è “considerato plausibile ma non è confermato”. Il bugiardino di AstraZeneca sarà aggiornato per includere i rari effetti collaterali e l’avvertimento di prestare attenzione alla comparsa di sintomi post vaccinazione come mal di testa persistente, vista appannata, ematoma nel luogo dell’iniezione. L’Ema tuttavia non ha imposto restrizioni sull’età o raccomandazioni, spiegando che la maggioranza dei casi di trombi rari è stata individuata in donne sotto i 60 anni entro due settimane dalla vaccinazione ma che non ha appurato rischi specifici connessi a fasce di età o sesso. “Potrebbe essere dovuto al fatto che più donne sono state vaccinate”, ha spiegato la dottoressa Sabine Straus. Inoltre per l’Agenzia europea del farmaco “non c’è modo di dire che la gravidanza o il contraccettivo orale possano essere fattori di rischio per questi casi specifici che abbiamo osservato”.Nel Regno Unito l’orientamento che si è scelto è diverso: pur condividendo la posizione dell’Ema sui benefici superiori ai rischi, l’ente regolatore britannico ha annunciato che agli under 30 sarà offerta la scelta di un vaccino alternativo ad AstraZeneca, cioè Pfizer o Moderna (sono questi tre infatti i rimedi in uso nel Paese, con le iniezioni di Moderna iniziate oggi). Al 31 marzo nel Paese si sono verificati 79 casi rari di coaguli nel sangue, con 19 morti, dopo la somministrazione del vaccino contro il coronavirus Oxford-AstraZeneca, e 3 di questi avevano meno di 30 anni. “Seguiremo l’indicazione aggiornata”, ha assicurato il premier britannico Boris Johnson. La palla passa agli Stati: su AstraZeneca “le autorità nazionali prenderanno le decisioni sulla base della situazione del loro Paese” e in particolare “della situazione pandemica, dei tassi di infezione, degli altri vaccini”, “ciò che cerchiamo di fare noi, e speriamo di farlo bene, è fornire tutte le informazioni disponibili sia sui benefici sia sui rischi”, ha spiegato la direttrice esecutiva dell’Ema, Emer Cooke. Parole a cui è seguito un appello Ue: “L’esperienza di AstraZeneca dimostra che il nostro sistema di farmacovigilanza funziona. Ma è essenziale che seguiamo un approccio coordinato in tutta l’Unione europea. Dobbiamo parlare con una sola voce in tutta l’Ue per aumentare la fiducia pubblica nelle vaccinazioni”, ha affermato la commissaria europea alla Salute, Stella Kyriakides, mentre i ministri della Sanità dell’Ue si sono riuniti subito dopo il briefing dell’Ema. I Paesi europei hanno assunto posizioni diverse sull’uso di AstraZeneca. La Francia ne raccomanda l’uso solo da 55 anni in su, la Germania lo usa per gli over 60. Norvegia e Danimarca (che non sono membri Ue) ne hanno sospeso l’uso. Mentre il Belgio, poche ore dopo il briefing dell’Ema ha limitato la somministrazione alle persone con età uguale o superiore a 56 anni. Il Regno Unito non ha mai sospeso l’uso di AstraZeneca. Questo vaccino, più economico e più facile da conservare rispetto a molti altri, è cruciale anche un pilastro del programma Covax sostenuto dall’Onu che mira a consentire la vaccinazione anche nei Paesi più poveri del mondo.
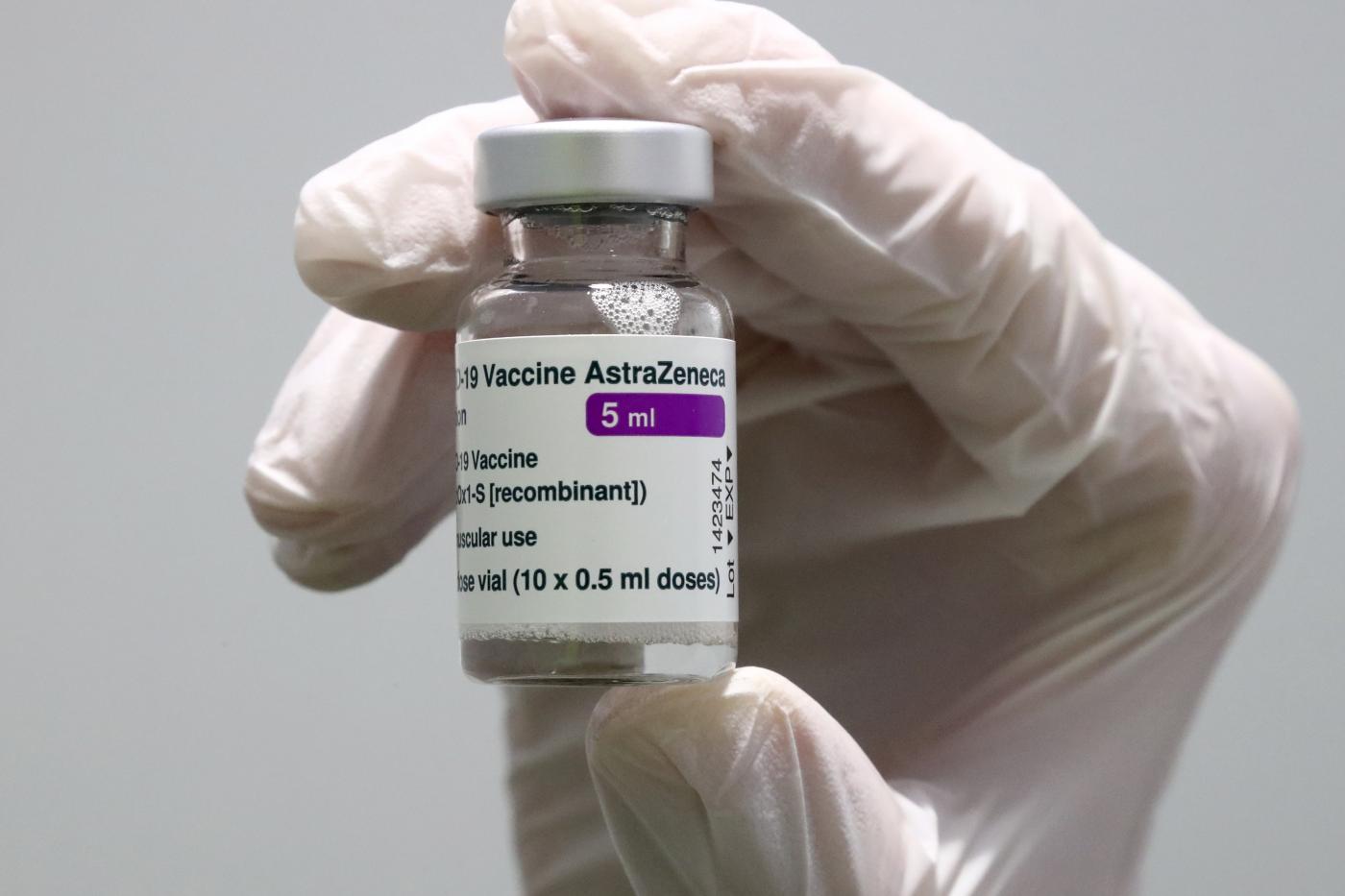
AstraZeneca, Ema: “Trombi sono effetto collaterale molto raro”
Seguici su
La conclusione dell’agenzia dopo 86 casi su 25 milioni di vaccinati
© Riproduzione Riservata

